UN ANTICANCÉREUX SPÉCIFIQUE
S'il existe des molécules capables de se fixer électivement aux ADN cancéreux, puis
de les
déstabiliser, d'autres substances, également douées d'affinité pour les ADN tumoraux,
doivent
pouvoir, au contraire, les stabiliser en resserrant les liens entre les brins
désappariés des chaînes.
Nous l'avons vu, les ADN cancéreux, déstabilisés, sont vulnérables et permettent à
de
nombreuses substances de se fixer à leurs brins écartés l'un de l'autre en de multiples
points.
Les cancérogènes vont étendre et augmenter cette séparation le long de la chaîne. A
partir des
sites d'initiation ainsi rendus disponibles, l'ADN polymérase peut accomplir son travail
de
réplication, l'ARN polymérase peut transcrire en ARN messager des gènes dont
l'expression
échappe aux régulations normales.
Les molécules anticancéreuses devront, elles aussi , être "attirées " par
les segments non
appariés des brins de l'ADN déstabilisé. Mais, cette fois, elles auront pour tâche de
créer, sans
toutefois former de liaisons irréversibles, une sorte de pont qui relie les brins entre
eux et
d' opposer en même temps un obstacle mécanique au fonctionnement des enzymes de
réplication et de transcription.
Ainsi, ne pouvant plus ni fonctionner, ni se renouveler, la cellule cancéreuse, qui
était devenue
dépendante de ses gènes déréglés, va mourir. La cellule en voie de transformation
cancéreuse
pourra, en revanche, retrouver un fonctionnement normal.
Bien entendu, la spécificité des nouveaux composés anticancéreux devra garantir
leur absence
d'action sur les cellules normales.
Tel était le raisonnement de Beljanski dès 1977. Or, depuis un an, il avait le moyen
de reconnâître
rapidement, grâce à l'oncotest, l'effet d'un composé sur les ADN cancéreux et normaux.
Il entreprit donc de tester de nombreuses molécules.
Une polémique avait été soulevée, à l'époque, au sujet de la réserpine:
largement employée
comme hypotenseur et comme sédatif, elle avait ensuite été soupçonnée d'être
cancérogène.
Beljanski s'y intéressa donc et, comme ce médicament est un des alcaloides extraits de
Rauwolfia serpentina, qui est une Apocynacée, son attention fut attirée sur cette
famille de
plantes riches en alcaloides.
Il soumit donc à l'Oncotest des extraits de diverses Apocynacées, contenant chacune
plusieurs
alcaloïdes; et il découvrit que certains d'entre eux se fixaient sélectivement sur les
ADN
cancéreux de mammifères et de plantes. Des alcaloides comme l'alstonine ou la
sempervirine,
isolés et purifiés, inhibaient fortement la synthèse in vitro des ADN cancéreux sans
pratiquement
affecter celle des ADN normaux. En outre, ils étaient capables de contrecarrer l'effet
déstabilisant des cancérogènes. Ils devaient donc pouvoir, in vivo, s'opposer au
développement
des tumeurs malignes et même à la transformation d'uné cellule normale en cellule
cancéreuse.
Beljanski et ses collaborateurs ont effectué une analyse très poussée des
propriétés de ces
remarquables alcaloïdes. Ils ont constaté qu'ils manifestent une très grande affinité
pour les
oligoribonucléotides riches en guanine et en adénine (nous avons vu que ce sont des
molécules
très actives au niveau de l'ADN: les amorceurs, les ARN transformants, les ARN
tumorigènes
sont tous riches en bases puriques).
Cette affinité est une propriété précieuse pour inhiber la réplication des ADN
cancéreux au
moyen des alcaloides choisis, car elle leur permet de se fixer soit aux amorceurs, ce qui
entrave
l'action de ces derniers, soit à des molécules d'ARN encore adhérentes à 1'ADN et
situées, par
exemple, juste à côté d'un site d'initiation. I1 faut noter à ce propos que, si l' on
en juge par
l' analyse de leurs amorceurs spécifiques, les sites d' initiation des ADN tumoraux ne
sont pas
les mêmes que ceux des ADN normaux; du reste, beaucoup plus de sites sont disponibles,
car
ils ont été mis à nu par l'écartement des brins de la châîne déstabilisée.
L'équipe a également montré que les alcaloïdes anticancéreux peuvent aussi
s'accrocher
directement à la molécule d'ADN à la faveur de l'écartement des brins; en effet, ils
entrent en
compétition avec les psoralènes, molécules bien connues pour se fixer aux brins d'ADN
de
manière à s'intercaler entre eux, et ils les chassent de cette localisation'l'.
Un brevet est accordé dès 1979, mais c'est en 1984 que Mirko et Monique Beljanski
publient une
note décrivant brièvement l'action de trois alcaloides anticancéreux spécifiques
(alstonine,
serpentine, sempervirine) sur la prolifération de cellules cancéreuses et de cellules
saines cultivées
in vitro. Les cellules cancéreuses, provenant de lignées humaines et animales bien
établies et stables
(KB, HeLa, Hep Il. L), ont toutes été tuées; les cellules normales de mammiferes (Vero,
RC, BHK)
n'ont pas été touchées. Une équipe belge a, l'année suivante, confirmé les
résultats de ces travaux.
Le BG-8 (alstonine), à base d'un alcaloide très actif et non toxique, fut mis au
point. Après
avoir démontré son effet anticancéreux in vitro, il fallait maintenant vérifier son
action in vivo.
Selon un protocole expérimental classique, il fut testé chez des souris porteuses de
lymphome,
d'ascite d'Ehrlich ou de tumeurs mammaires. Le critère d'efficacité choisi consistait à
obtenir
à la suite du traitement une survie de trois mois en excellente condition physique. Le
BG-8
permit d' atteindre 80 à 90 % de guérisons et parfois plus. Les doses nécessaires
étaient faibles.
Aucun effet secondaire toxique ne se manifesta.
Très rapidement, Beljanski eut l'idée d'améliorer encore les résultats in vivo en
associant un
traitement classique très léger à l'utilisation du BG-8. Pourquoi ? Parce qu'à faible
dose, les
antimitotiques et la radiothérapie, en déstabilisant les ADN cancéreux, en séparant
les brins de
leurs chaînes, mettent à nu des sites d'initiation supplémentaires auxquels le
médicament va
pouvoir se fixer; cela facilite et renforce son action.
Les résultats ont été excellents . Pour démontrer l' intérêt d' une association
des deux types de
traitement, une série d'expériences fut entreprise chez la souris atteinte du dangereux
lymphome YC-8. L'équipe se plaça volontairement dans des conditions très défavorables
en
administrant des doses trop faibles de BG-8 et d'antimitotique. Alors que les animaux
témoins
étaient tous morts dès le trentième jour, la survie à 90 jours était, avec le BG-8
seul, de 30 %,
et, avec le CCNU seul, de 45 %; mais avec l'association du BG-8 et du CCNU, elle atteignit
100 %. D'autres essais similaires ont été menés avec succès en associant au BG-8 le
5-FtJ,
l'Endoxan ou la daunorubicine.
De très nombreuses expériences ont montré que le BG-8 ne se fixe ni à l'ADN normal,
ni à
quelque autre niveau des cellules saines. Il est totalement dénué de toxicité, en
particulier pour
les cellules sanguines. Les animaux guéris ont survécu en excellent état, sans perdre
de poids
ni éprouver d' effets secondaires indésirables. Le BG-8 a, d' autre part, empêché les
antimitotiques ou la radiothérapie d'exercer des actions nocives.
(1) L'utilisation des psoralènes pour le bronzage artificiel a été vivement
contestée récemment, car leur potentiel
cancérogène a été démontré.
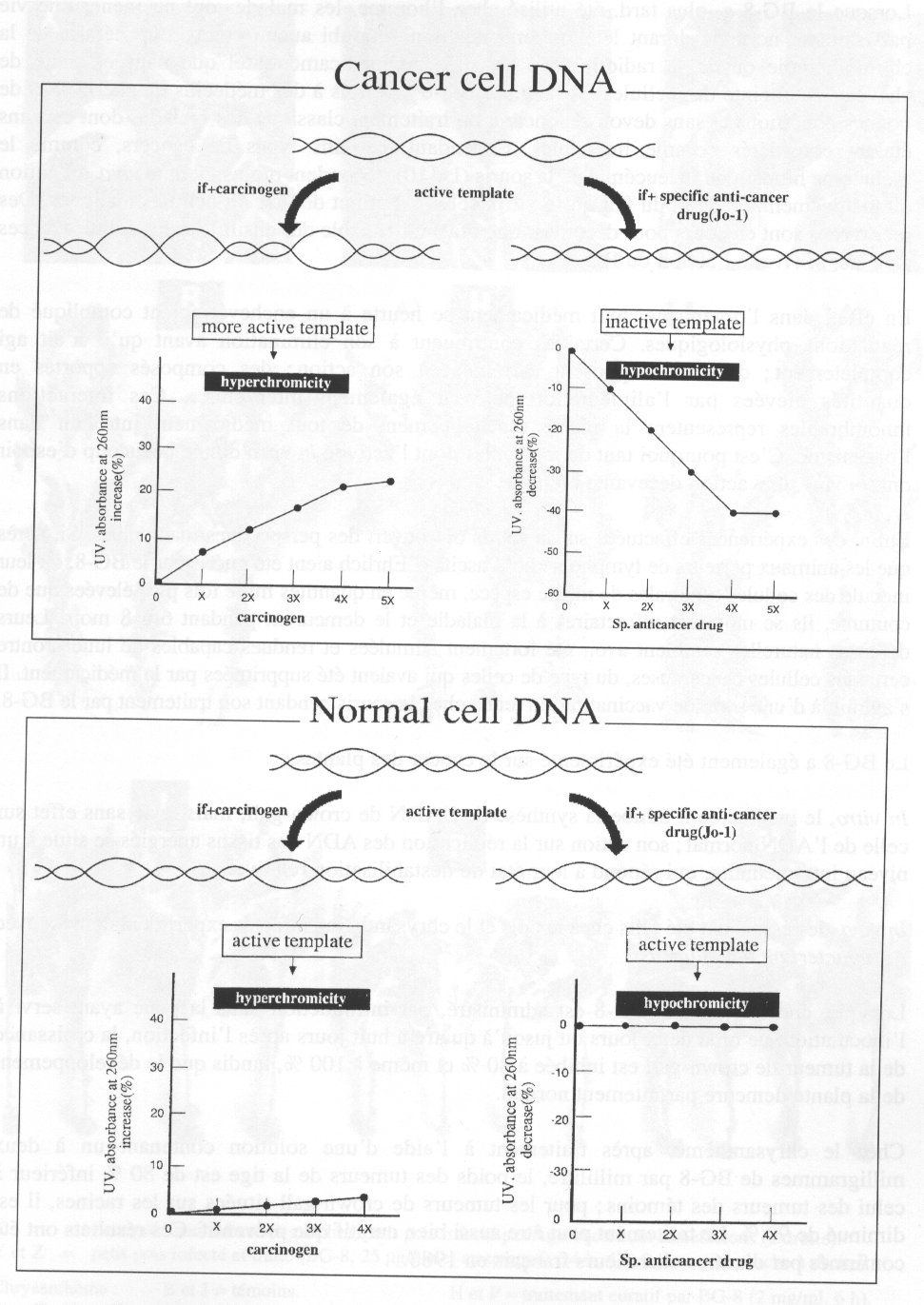
< IMG_P61.JPG >

Comportement d'ADN cancéreux et d'ADN normaux dans l'Oncotest
Lorsque le BG-8 a, plus tard, été utilisé chez l'homme, les malades ont pu mener une
vie
parfaitement normale durant leur traitement; ils n'ont subi aucun contrecoup néfaste de
la
chimiothérapie ou de la radiothérapie associée au médicament, tel que nausée, chute
de
cheveux ou atteinte des cellules du sang. Le BG-8 a permis à des médecins de guérir
dans de
bonnes conditions et sans devoir renoncer à un traitement classique des malades dont
certains
étaient considérés comme incurables. Cependant, certains types de cancers, comme le
mélanome humain ou la leucémie de la souris (L 110), répondent moins bien, in vivo, à
1' action
du médicament, en dépit du fait qu'in vitro, celui-ci permet de tuer les cellules
malignes. Des
recherches sont en cours pour découvrir un cofacteur capable de sensibiliser les cellules
de ces
cancers, in vivo, à l'action du BG-8.
En effet, dans l'organisme, tout médicament se heurte à un enchevêtrement compliqué
de
régulations physiologiques. Certaines contribuent à son élimination avant qu'il n'ait
agi
complètement; d'autres s'opposent carrément à son action; des composés apportés en
quantités élevées par 1' alimentation peuvent également intervenir. . . Ces
interactions
innombrables représentent la pierre d'achoppement de tout médicament introduit dans
l'organisme. C'est pourquoi tant de molécules dont l'activité in vitro donne beaucoup
d'espoir
ont, in vivo, une action décevante ou nulle.
Enfin, des expériences effectuées sur la souris ont ouvert des perspectives
inattendues. Si, après
que les animaux porteurs de lymphome ou d'ascite d'Ehrlich aient été guéris par le
BG-8, on leur
inocule des cellules tumorales de même espèce, même en quantités mille fois plus
élevées que de
coutume, ils se montrent réfractaires à la maladie et le demeurent pendant 6 à 8 mois.
Leurs
défenses naturelles semblent avoir été fortement stimulées et rendues capables de
lutter contre
certCunes cellules cancéreuses, du type de celles qui avaient été supprimées par le
médicament. I1
s'agirait là d'une sorte de vaccination survenue chez la souris pendant son traitement
par le BG-8.
Le BG-8 a également été expérimenté sur le cancer des plantes.
In vitro, le médicament inhibe la synthèse de l'ADN de crown-gall, mais reste sans
effet sur
celle de l'ADN normal; son action sur la réplication des ADN des tissus anergiés se
situe à un
niveau intermédiaire, qui répond à leur état de déstabilisation relative.
In vivo, des essais ont été faits chez le pois et le chrysanthème infectés
expérimentalement avec
Agrobacterium tumefaciens.
Lorsque, chez le pois, le BG-8 est administré, par introduction dans la plaie ayant
servi à
l'inoculation, de un à deux jours ou jusqu'à quatre à huit jours après l'infection, la
croissance
de la tumeur de crown-gall est inhibée à 80 % et même à 100 %, tandis que le
développement
de la plante demeure parfaitement normal.
Chez le chrysanthème, après traitement à l'aide d'une solution contenant un à deux
milligrammes de BG-8 par millilitre, le poids des tumeurs de la tige est de 80 %
inférieur à
celui des tumeurs des témoins; pour les tumeurs de crown-gall situées sur les racines,
il est
diminué de 90 %. Le traitement peut être aussi bien curatif que préventif. Ces
résultats ont été
confirmés par d'autres chercheurs français en 1983.
I1 existe une relation très étroite entre le développement des tissus de crown-gall
et l'effet in
vitro du BG-8 sur leur ADN: diminution du degré de séparation des chaînes et arrêt de
la
réplication.
< IMG_P63.JPG >
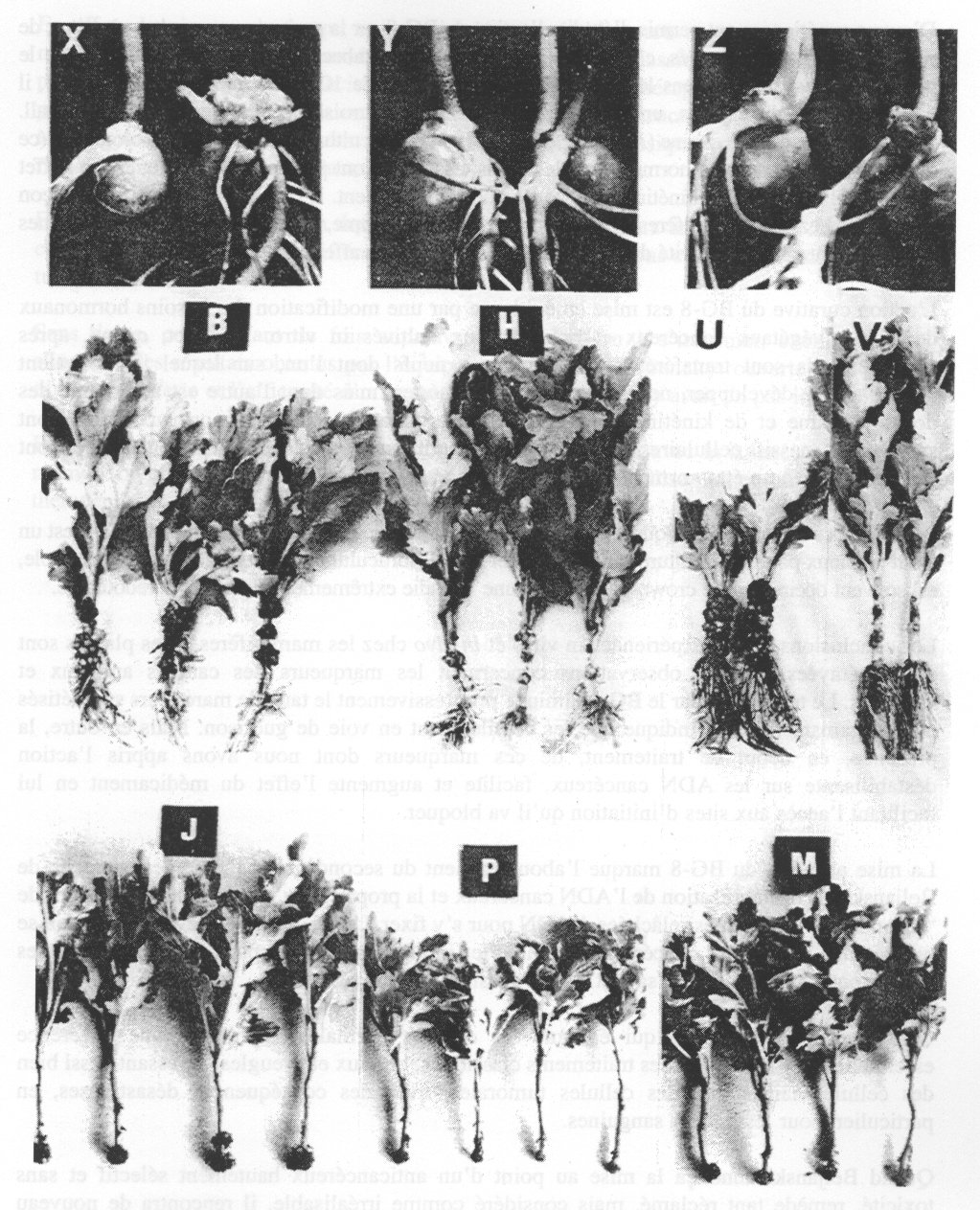
X = petit pois non infecté (à gauche), petit pois infecté par
Agrobacterium tumefaciens (à droite).
Y et Z = petit pois infecté et traité (BG-8, 25 ,ug/plaie) au temps 0, 24 h, 4 et 8
jours (de gauche à droite).
Chrysanthème: B et J = témoins.
H et P = traitement curatif par BG-8
(2 mg/ml, 6 h).
V et M = traitement préventif. U et J = témoins.
B H U et V = Ch.c.v. Marquis J P et M = Ch.c. v. Padoux (réf.94).
D' autres expériences ont permis d'étudier l' action du BG-8 sur la croissance, en
culture in vitro, de
tissus cancéreux et anergiés, c'est-à-dire précancéreux, de tabac et de vigne vierge.
Lorsque le
médicament est présent dans le milieu de culture à raison de 10 microgrammes par
millilitre, il
provoque, en quinze jours, une inhibition à 75 % de la croissance des tissus de
cronvn-gall.
Cependant, lorsqu'une auxine (AIA) est ajoutée au rnilieu de culture à des doses
physiologiques (ce
qui équivaut à un excès d'hormone, car les tissus testés n'en ont pas besoin), elle
neutralise l'effet
antitumoral du BG-8. La kinétine, elle, ne l'entrave aucunement. I1 faut souligner que
d'une façon
similaire, chez les mammiferes et en particulier chez l'homme, une hypersécrétion
d'hormones
stéroides contrecarre l'activité du médicament sur les cancers affectant leurs
cellules-cibles<2>.
L' action curative du BG-8 est mise en évidence par une modification des besoins
hormonaux
des tissus végétaux cancéreux et précancéreux cultivés in vitro. En effet, quand,
après
traitement, ils sont transférés sur des milieux neufs dont l'un, sur lequel ils
pouvaient
auparavant se développer, ne contient pas d'hormones, mais dont l'autre est additionné
des
doses d'auxine et de kinétine requises pour la croissance des tissus normaux, seuls vont
survivre les massifs cellulaires placés sur ce second milieu: les cellules autrefois
malades sont
donc revenues à un état normal, sain.
Intéressants sur le plan théorique, ces résultats ont une grande importance
pratique: le BG-8 est un
atout précieux pour l'agriculture et en particulier pour l'horticulture; le
chrysanthème, par exemple,
est souvent décimé par le crown-gall, qui est une maladie extrêmement répandue et
redoutable.
Le s conclusions de ces expériences in vitro et in vivo chez le s mammifères et les
plantes sont
encore étayées par des observations concernant les marqueurs des cancers animaux et
végétaux. Le traitement par le BG-8 diminue progressivement le taux de marqueurs
synthétisés
par l'organisme, ce qui indique que les cellules sont en voie de guérison. Mais en outre,
la
présence, en début de traitement, de ces marqueurs dont nous avons appris l' action
déstabilisante sur les ADN cancéreux, facilite et augmente l'effet du médicament en lui
facilitant l'accès aux sites d'initiation qu'il va bloquer.
La mise au point du BG-8 marque l'aboutissement du second grand thème de recherche de
Beljanski: la déstabilisation de l'ADN cancéreux et la propriété qu'ont certaines
molécules de
"reconnaître" les chaînes relâchées d' ADN pour s ' y fixer. Le BG-8 paraît
"savoir" qu 'il doit se
rendre dans les cellules cancéreuses, comme les molécules utilisées par l'organisme
pour ses
régulations physiologiques "savent", elles aussi, où se diriger.
Cette spécificité d'action, qui épargne les cellules normales, représente une
différence
es sentielle entre le B G - 8 et le s traitements clas sique s , brutaux et aveugles ,
agres sant aus si bien
des cellules saines que des cellules tumorales, avec des conséquences désastreuses, en
particulier, pour les lignées sanguines.
Quand Beljanski annonça la mise au point d'un anticancéreux hautement sélectif et
sans
toxicité, remède tant réclamé, mais considéré comme irréalisable, il rencontra de
nouveau
l'incompréhension et l'hostilité.
Cependant, en 1985, la revue de l'Université Paris-Sud, où se trouvait son
laboratoire, lui
demanda un article dans lequel il put résumer les théories et les expériences qu'il
avait publiées
au cours des années précédentes.
(2) il en va de même d'un excès de stérols d'origine alimentaire, qui peuvent être
transformés par l'organisme en
hormone stéroïdes.
En effet, depuis peu de temps, un certain désarroi était apparu au sein de la
communauté
médicale. Certains des plus grands noms de la cancérologie classique commençaient à
mettre
publiquement en doute l'efficacité à long terme de la chimiothérapie et de la
radiothérapie et
préconisaient le recours à des composés naturels, moins destructeurs. Quelques
spécialistes
allèrent jusqu'à prôner l'abandon total des thérapeutiques classiques; mais ils ne
proposaient
rien de concret pour les remplacer.
Entre-temps, Beljanski et son équipe avaient préparé plusieurs anticancéreux
sélectifs, dont
certains d'un mode d'action différent de celui du BG-8, mais tous capables de stabiliser
1'ADN
tumoral.
Sans doute, comme tant de fois auparavant, cherchait-on à s'informer, éventuellement
à
s'inspirer des résultats obtenus par l'équipe; mais de là à reconnaître ouvertement
la valeur
d'une découverte et l'efficacité d'un remède révolutionnaire, il y avait un pas
infranchissable.
Beljanski serait-il destiné à se trouver toujours en opposition avec la science
officielle ? Au
moment où elle parle d'abandonner les antimitotiques, il les utilise, lui, comme adjuvant
à sa
thérapeutique. . .
RÉSUMÉ
Puisqu' il existe des molécules capables de se fixer électivement à l' ADN
cancéreux
pour le déstabiliser, d'autres substances, pense Beljanski, doivent au contraire
pouvoir s'accrocher spécifiquement à cet ADN pour le stabiliser en liant à nouveau
entre eux les brins séparés des châînes.
A l' aide de l' Oncotest, il recherche donc des produits "attirés"
spécifiquement par les
segments désappariés des ADN déstabilisés, mais sans action sur les ADN normaux.
Des alcaloides extraits de certaines plantes s'avèrent capables, in vitro, d'inhiber
fortement la synthèse des ADN cancéreux, mais de n'affecter pratiquement pas celle
des ADN normaux; en outre, ils peuvent contrecarrer l'effet déstabilisant des
cancérogènes sur les ADN tumoraux.
L' action de ces alcaloides s' exerce au niveau des amorceurs et des sites d'initiation
spécifiques des ADN tumoraux.
Le BG 8 (Alstonine), médicament anticancéreux spécifique dénué d'action sur les
cellules normales, très actif et non toxique, est mis au point. Après avoir été testé
in
vitro, en particulier sur des cultures de cellules, il subit avec un égal succès les
essais
in vivo chez la souris atteinte de divers cancers, conduisant à 80 ou 90 % de guérisons
et parfois plus.
Les résultats sont encore améliorés lorsqu'une radiothérapie ou une chimiothérapie
à
dose faible est associée au BG 8: en effet, ces agents thérapeutiques classiques
accentuent l'ouverture des châînes de l'ADN tumoral, permettant au médicament
d'accéder à un plus grand nombre de sites d'initiation, qu'il va bloquer.
Le BG-8 empêche les traitements antitumoraux classiques d'exercer leurs effets
secondaires nocifs. Les malades qui, après une longue expérimentation du produit
chez l'animal, ont reçu du BG-8 ont pu mener une vie normale pendant ce traitement
et n'ont subi aucun contrecoup néfaste des thérapeutiques classiques qui y étaient
associées.
Le BG-8 s'est montré effficace contre un très grand nombre de cancers humains et
animaux. Il a permis également de guérir des plantes atteintes de crown-gall;
extrêmement répandue, cette maladie est particulièrement redoutable pour
l' horticulture.
L' action du BG 8 est néanmoins contrecarrée par la présence d'un excès d'hormones
qui déstabilisent l'ADN: hormones stéroïdes chez l'animal et l'homme, auxines chez
les végétaux.
Contrairement aux traitements classiques, brutaux et aveugles, qui détruisent sans
distinction toute cellule en division rapide, malade ou saine, le BG-8 attaque
uniquement et spécifiquement les cellules tumorales. Il permet de tuer les cellules
cancéreuses et de ramener à la normale les cellules précancéreuses.